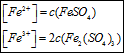Př.
39 Měrná platinová elektroda byla ponořená do roztoku, který vznikl smícháním
40 ml roztoku FeSO4 o koncentraci 0,01 mol/l a 10 ml roztoku Fe2(SO4)3
o koncentraci 0,1 mol/l.
E0(Fe3+/Fe2+) = 0,77 V, R = 8,314 J
mol-1 K-1,
F = 96485 C mol-1, hodnota 2,303.RT/F je při teplotě 25°C rovna
0,0592 V.
a) Napište Nernstovu rovnici pro platinovou měrnou
elektrodu ponořenou do směsného roztoku FeSO4 a Fe2(SO4)3.
b) Jaký rovnovážný potenciál má platinová
elektroda v tomto směsném roztoku?
c) Jaké bude elektromotorické napětí článku,
složeného z měrné platinové elektrody a referentní nasycené
kalomelové elektrody (SKE), ponořeného v tomto roztoku. E(SKE) = 0,246 V?
Řešení:
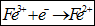
 kde z = 1, protože 1
elektron se vyměňuje
kde z = 1, protože 1
elektron se vyměňuje
| b) |
|
|
|
| 2,303RT/F |
0,0592 |
V |
|
| E0(Fe3+/Fe2+) |
0,77 |
V |
|
| V(FeSO4) |
0,04 |
l |
|
| c(FeSO4) |
0,01 |
mol/l |
|
| V(Fe2(SO4)3) |
0,01 |
l |
|
| c(Fe2(SO4)3) |
0,1 |
mol/l |
|
|
|
|
|
| n(FeSO4)=c*V |
0,0004 |
mol |
|
| n(Fe2(SO4)3)=c*V |
0,001 |
mol |
|
| c(FeSO4)=n/Vcelk |
0,008 |
mol/l |
|
| c(Fe2(SO4)3)=n/Vcelk |
0,02 |
mol/l |
|
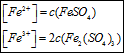 |
|
|
|
|
|
|
|
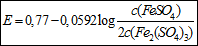 |
= 0,811 V |
|
|
|
|
|
|
|
|
|
|
| c) |
|
|
|
| E(SKE) |
0,246 |
V |
|
|
|
|
|
| EMN=E(+) - E(-) |
0,565 |
V |
|
 kde z = 1, protože 1
elektron se vyměňuje
kde z = 1, protože 1
elektron se vyměňuje