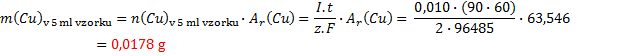
Př.
44 Obsah
mědi ve vzorku byl stanoven coulometricky za konstantního proudu. Vzorek o hmotnosti
10 g byl rozpuštěn v H2SO4, převeden do odměrné
baňky o objemu 250 ml a doplněn destilovanou vodou po rysku. Do
coulometrické cely byl přidán základní elektrolyt a bylo pipetováno 5 ml
připraveného vzorku, který obsahoval stanovenou měď ve formě CuSO4.
Analýza, během které se na katodě vyloučila měď, proběhla při
proudu 10 mA po dobu 1 hod 30 min.
F
= 96485 C mol-1, M(Cu) = 63,546 g mol-1
a) Napište rovnici elektrochemického děje na katodě.
b) Vypočítejte hmotnost mědi, která se vyloučí na katodě během analýzy
5 ml vzorku.
c) Vypočítejte hmotnostní zlomek mědi v původním vzorku.
Řešení:
a) Cu2+ + 2 e- ---> Cu
b)
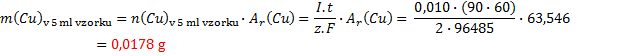
c) celkové množství mědi ve vzorku, tedy množství mědi ve 250 ml je padesáti násobek
hodnoty z bodu b)
![]()
a hmotnostní zlomek mědi ve vzorku
![]()